На прошлых уроках мы с вами говорили о том, что существует три агрегатных состояния вещества — твёрдое, жидкое и газообразное.
И выяснили, что при агрегатных превращениях возможны переходы вещества из одного агрегатного состояния в другое.
На этом уроке мы рассмотрим процесс превращения жидкости в газ, и обратное превращение вещества из газообразного состояния в жидкое.
Задумывался ли кто-нибудь из вас над вопросом: почему сохнет мокрая одежда? И почему в ветреную погоду она высыхает значительно быстрее, чем в тихую и прохладную? А если оставить открытым флакон духов, то очень скоро он может оказаться пустым. Почему? Попытаемся ответить на эти и некоторые другие вопросы.
Для начала давайте вспомним, что молекулы вещества в любом его агрегатном состоянии находятся в непрерывном движении. Их скорости меняются самым случайным образом.
Так, например, молекула жидкости, имеющая большую скорость, несомненно обладает и большой кинетической энергией. Такая молекула может преодолеть силы притяжения к другим молекулам и покинуть жидкость. А так как молекулы с большой энергией есть всегда, то со временем количество жидкости будет уменьшаться, а над жидкостью будет образовываться пар.

Явление превращения жидкости в пар называется парообразованием.
Водяной пар невидим. А то, что мы свами часто ошибочно называем паром — например, белёсую струю, выходящую из кипящего чайника, — это не пар, а туман. Он состоит из крошечных капелек воды, образовавшихся при конденсации пара. Но об этом явлении мы поговорим позже.
Отличают два вида парообразования — это испарение и кипение. Они осуществляются при разных условиях.
Испарение — это парообразование, идущее со свободной поверхности жидкости.
А от чего зависит скорость испарения жидкости? Чтобы ответить на этот вопрос, давайте с вами проведём следующий опыт. На стекло нанесём тампоном влажные пятна одинаковых размеров в такой последовательности: подсолнечное масло, вода, ацетон. И проследим, какая жидкость испарится первой.

Через некоторое время мы заметим, что первым исчезнет пятно ацетона, затем воды, и позже всех — подсолнечного масла. Следовательно, скорость испарения зависит от рода жидкости. Это и понятно, ведь у разных жидкостей силы взаимодействия молекул неодинаковые.
Продолжим опыт. Одну стеклянную пластинку возьмём холодную, а другую нагреем. И нанесём на них две одинаковые капли воды.

С нагретого стекла капля исчезнет быстрее, чем с холодного.
И это неудивительно, поскольку чем выше температура жидкости, тем больше скорость движения её молекул, и, соответственно, их кинетическая энергия. Следовательно, большее число молекул способно преодолеть силы притяжения и выйти за пределы поверхности жидкости.
Значит, скорость испарения жидкости зависит от её температуры: чем она выше, тем скорость испарения жидкости больше.
А теперь капнем на стекло две капли ацетона. Размажем одну каплю так, чтобы образовалось пятно, и проследим за изменениями.

Через некоторое время мы заметим, что пятно ацетона испарится быстрее, чем капля. Это объясняется тем, что площадь поверхности пятна больше, чем капли. Следовательно, большее число молекул сможет оказаться на поверхности и, преодолев силы притяжения, вылететь из неё. Значит, чем больше площадь свободной поверхности жидкости, тем больше скорость её испарения.
И наконец, на два стекла нанесём по капле воды, но одно стекло будем обдувать вентилятором.
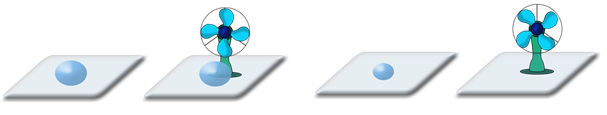
Капля со стекла, обдуваемого вентилятором испарится гораздо быстрее. Почему? Всё дело в том, что при испарении молекулы не только покидают поверхность жидкости, но и возвращаются обратно. А поток воздуха уносит вылетевшие из жидкости молекулы, освобождая место другим. Таким образом, скорость испарения зависит от движения воздуха над свободной поверхностью жидкости.
А теперь выясним, что же происходит с жидкостью в сосуде при испарении. Для этого проделаем такой опыт. Возьмём термометр и обмотаем его конец ватой, смоченной водой, а лучше спиртом.
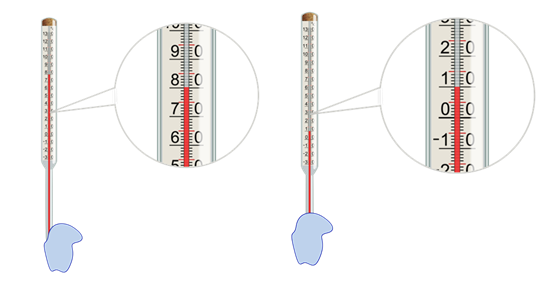
Мы практически сразу заметим, как столбик жидкости в термометре начнёт опускаться. Это свидетельствует об уменьшении температуры жидкости при испарении.
Объясняется этот факт следующим образом. При испарении жидкость покидают молекулы, обладающие наибольшей энергией. Это означает, что внутренняя энергия оставшейся части жидкости уменьшается. Поэтому, если нет притока энергии к жидкости извне, температура испаряющейся жидкости уменьшается.
Мы рассмотрели процессы испарения жидкостей. Однако у вас может возникнуть закономерный вопрос: «А испаряются ли твёрдые тела?».
Для ответа на него, проведём следующий опыт. Поместим в пробирку кристаллики йода и будем нагревать над пламенем спиртовки. Через некоторое время мы заметим, как кристаллики йода начнут испаряться.
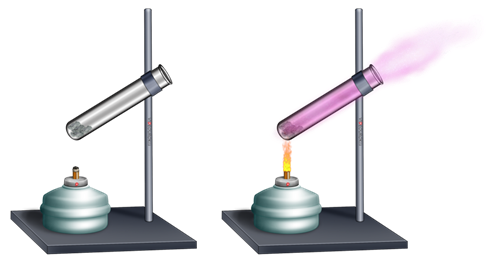
Значит, твёрдые тела тоже испаряются. Этим и объясняется то, что в ясный морозный день исчезает иней на деревьях, а бельё способно высохнуть даже в очень сильный мороз.
В самом начале мы говорили о том, что очень часто люди ошибочно называют паром туман, который состоит из крошечных капелек воды.

Так же все вы не раз наблюдали, как вечером, после жаркого летнего дня, выпадает роса. Это водяной пар, содержащийся в воздухе, при охлаждении превращается в жидкость, и капельки воды оседают на листьях и траве.
Процесс превращения вещества из газообразного состояния в жидкое называют конденсацией (от латинского «сгущать»).
Если процесс испарения идёт быстрее, чем процесс конденсации, то масса жидкости в сосуде уменьшается. Но почему тогда в плотно закрытой банке с водой уровень воды остаётся неизменным? Разве в закрытом сосуде молекулы не вылетают из воды?
Вылетают, конечно. Но из закрытого сосуда они вылететь не могут, поэтому, полетав над жидкостью, многие молекулы возвращаются обратно в жидкость. То есть одновременно с испарением происходит и конденсация.
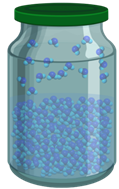
А то, что уровень жидкости в закрытом сосуде остаётся неизменным, означает, что в таком сосуде процессы парообразования и конденсации идут с одинаковой скоростью. Говорят, что в этом случае наступает динамическое равновесие между жидкостью и паром. При динамическом равновесии масса жидкости в закрытом сосуде не изменяется, хотя жидкость продолжает испарятся.
Пар, находящийся в состоянии динамического равновесия со своей жидкостью, называется насыщенным паром.
Пар, который не находится в состоянии динамического равновесия со своей жидкостью, называют ненасыщенным паром.
А теперь давайте поставим наш закрытый сосуд, в котором жидкость и пар находятся в состоянии динамического равновесия, над спиртовкой и будем нагревать его.
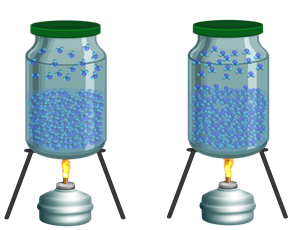
При увеличении температуры, количество молекул, способных вылететь с поверхности жидкости, возрастает. Поэтому в начале количество молекул, покидающих жидкость, будет больше, чем тех, которые возвращаются обратно. Соответственно, нарушается динамическое равновесие и пар перестаёт быть насыщенным.
Однако через какое-то время равновесие вновь восстановится. Но так как число молекул в единице объёма пара увеличится, то увеличится и плотность насыщенного пара. А мы уже знаем, что при увеличении плотности газа возрастает и его давление. Значит, с увеличением температуры, плотность и давление насыщенного пара увеличиваются.
Домашнее задание
Стр. 47 — 50 читать