Агрегатные состояния вещества
Радость видеть и понимать –
есть величайший дар природы
Альберт Эйнштейн
Данная тема посвящена изучению различных состояний вещества. Известно, что вода может находиться в трех состояниях: твердом, жидком и газообразном. То есть, при достаточно низких температурах вода становится льдом или снегом. И, наоборот, при достаточно высоких температурах, вода превращается в пар. Это, конечно, присуще не только воде, но и другим веществам. Итак, любое тело может быть твердым, жидким или газообразным. В зависимости от состояния, тела обладают различными свойствами. Известно, что твердые тела имеют собственную форму и сохраняет объём. Например, стол или стул – это твердые тела, поскольку они имеют определенную форму, которую сохраняют и занимают определенный объём. Для того чтобы изменить форму твердого тела, нужно приложить большое усилие. Например, практически невозможно согнуть или расплющить монету руками. Однако если по ней ударить молотком, то можно её расплющить. Другой пример: стеклянный стакан тоже сохраняет свой объем и форму. Конечно, стакан довольно легко разбить: чаще всего, достаточно просто уронить его на пол. Жидкости, напротив, легко меняют свою форму. Разумеется, это легко доказать, если переливать воду в емкости различной формы: вода будет принимать форму того сосуда, в который она помещена. Тем не менее, жидкости сохраняют свой объём. Это тоже легко проверить: если наполнить бутылку до краев водой и попробовать перелить эту воду в стакан, который явно поменьше. Можно убедиться, что вода туда не поместится: либо в бутылке останется немного воды, либо вода польётся через край стакана.
Газы не сохраняют ни форму, ни объём. Большинство газов прозрачны и бесцветны, а потому невидимы. Достаточно известен один пример газа – это воздух. Конечно, можно перемещаться по комнате, не испытывая никаких затруднений с дыханием. Значит, воздух заполняет всю комнату.
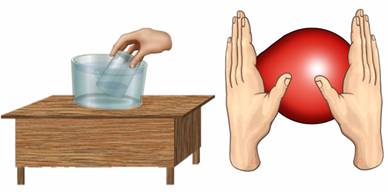
Если попробовать поднять стакан вверх дном и опустить его в воду, то вода его не заполнит. Почему? Потому что там воздух. Ранее был рассмотрен пример с воздушным шариком: можно без труда изменить объём и форму шарика, несмотря на то, что количество газа внутри шарика не меняется. Итак, газы не сохраняют ни свою форму, ни свой объём. Они принимают форму сосуда и заполняют весь предоставленный объём.
Одно и то же вещество может находиться в различных состояниях в зависимости от внешних условий (в основном, это температура).
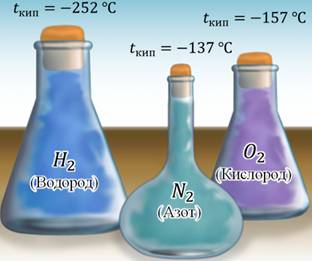
Например, водород закипает уже при температуре минус 252 градуса Цельсия (°С). Конечно, такую температуру на Земле можно получить только в лабораторных условиях и то, это довольно не просто. Газ азот (который является основной составляющей воздуха) становится жидким только при температуре минус 137°С, а кислород – при температуре минус 157°С. Поэтому, данные вещества практически всегда находятся в газообразном состоянии на нашей планете. Металлы – наоборот, почти всегда находятся в твердом состоянии. Дело в том, что для того, чтобы перевести их в жидкое состояние, нужны высокие температуры. Например, чтобы расплавить железо, нужно более полутора тысяч градусов Цельсия. Чтобы расплавить медь нужно нагреть её до температуры около тысячи ста градусов Цельсия. Такие температуры достигаются на различных заводах и фабриках, которые производят изделия из металлов.
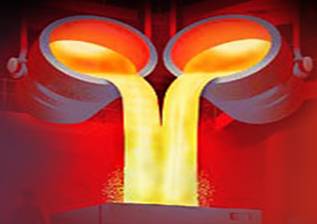
Люди используют свойство жидкости – легко менять свою форму. После того, как металлы переходят в жидкое состояние, их заливают в нужную форму, а потом остужают, чтобы они снова стали твердыми.
Изменение агрегатных состояний вещества постоянно происходит на нашей планете. Это отлично демонстрируется таким явлением, как круговорот воды в природе. Вода испаряется из водоемов, и водяные пары уносятся в атмосферу. Там они остывают, образуя облака и тучи. В конце концов, вода снова переходит в жидкое состояние и возвращается на Землю в виде осадков. Важно понимать, что изменение агрегатных состояний вещества не влечет за собой изменение молекул. Молекулы льда, воды и водяного пара абсолютно одинаковы: они состоят из двух атомов водорода и одного атома кислорода.
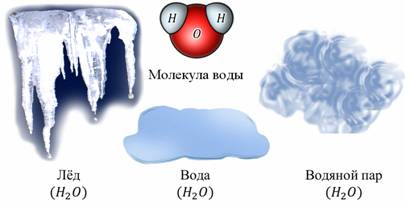
Поэтому, ни в коем случае нельзя путать изменение самого вещества с изменением его состояния. Различные агрегатные состояния вещества определяются расположением молекул, их движением и характером взаимодействия. Но об этом будет подробно рассказано в следующей теме.
Основные выводы:
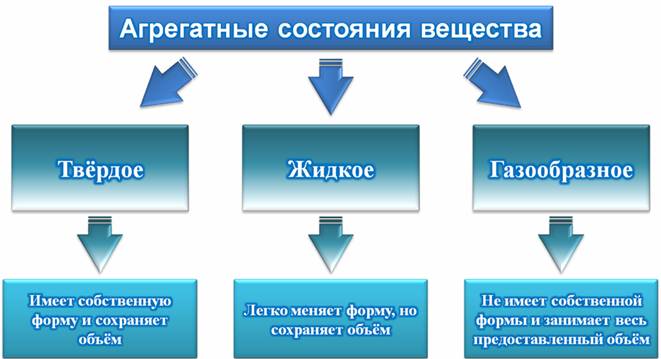
– Все вещества могут находиться в трех агрегатных состояниях: твердом, жидком и газообразном.
– Твердые тела имеют собственный объём и сохраняют форму.
– Жидкости легко меняют форму, но при этом сохраняют объём.
– Газы не имеют своей формы и занимают весь предоставленный объём (то есть, не сохраняют ни объём, ни форму).
– Вещество переходит в то или иное агрегатное состояние в зависимости от внешних условий.
Домашнее задание.
—